Cardiovascular Safety of Febuxostat or Allopurinol in Patients with Gout
White WB et al. CARES investigators.
NEJM 2018
PMID: 29527974
ClinicalTrials.gov number: NCT01101035.
資金提供Funding
開示Disclosures
私的背景
2017年 11月 15日 FDAからフェブキソスタット(フェブリク®️)についてSafety Alertsが発信された。その後、以下のサイトにあるように2019年2月21日フェブリク®️に枠組み警告がなされた。 FDA adds Boxed Warning for increased risk of death with gout medicine Uloric (febuxostat) 実は新薬としてフェブリク®️が承認された際に FDAから追加試験を実施するよう勧告されていた。日本時間 2018年 3月 12日に最新論文が NEJMに掲載された。早速、批判的吟味してみた。 結論 プライマリー・アウトカムはフェブキソスタット群とアロプリノール群との間に有意な差はなかった。セカンダリー・アウトカムではあるが、全死亡と心血管死についてはフェブキソスタットの方が多かった。ここまでは FDAの Alerts通り。 本試験は ITT解析であるが、脱落が多い点が気になる。また患者背景はかなりの肥満。
組入基準
1. 50歳以上の男性または 55歳以上の女性の患者で、アメリカリウマチ協会基準の1つまたは複数に基づいて、痛風と診断された患者。 a)化学または偏光顕微鏡法による尿酸結晶を含むことが証明された痛風結節および/または b)関節液中の特徴的な尿酸結晶および/または c)以下の少なくとも6つの病歴:一関節内関節炎、痛み/腫脹した第1中足趾節関節、片側第1中足趾節関節痛、片側足根関節痛、痛風結節、高尿酸血症、X線上の非対称腫脹、X線による侵食のない皮質嚢胞、関節炎発作時の生物体に対する陰性関節培養液。
2. 主要な心臓血管または脳血管疾患の病歴 以下のうちの少なくとも1つを含む: •心筋梗塞 •不安定狭心症による入院 •冠状動脈または脳血管再生術 •ストローク •一過性虚血性発作による入院 •末梢血管疾患(足首:上腕索指数<0.6、末梢動脈血行再建術および/または断続的跛行の十分に文書化された経過) •微小血管または大血管疾患(網膜症、神経障害、腎症、および小血管血管疾患)の証拠を有する真性糖尿病
3. スクリーニング来院時の血中尿酸値> 7.0mg / dl以上、血清尿酸値> 6.0mg / dl、不適切に管理された痛風(スクリーニング前の12ヶ月間の1回以上のフレアおよび/または痛風結節の存在)
4. 患者または被験者の法的に容認される代表者は、調査手続の開始前に書面によるインフォームドコンセントを提供することができる。
5. 被験者は、スケジュールされた診療所の予定を含むプロトコル要件を理解し、それに従うことができる。
除外基準
1.患者は、二次性高尿酸血症(例えば、骨髄増殖性疾患のため)を有する。
PICOTS
P : 心血管疾患を有する痛風患者(65歳くらい、BMI 33超、ハイリスク)
批判的吟味
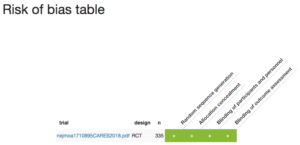
RobotReviewerによる Risk of Bias Table

ランダム割り付けされているか?(観察者バイアスはないか?)
されている
ブラインドされているか?(マスキングにより観察者バイアスは抑えられているか?)
されている(患者、医師、エンドポイント評価委員、データ解析者)
隠蔽化されているか?(選択バイアスはないか?)
プライマリーアウトカムは真か?明確か?
代用のアウトカムも含まれているが、ブラインドなので問題なさそう。しかし複合エンドポイントであるため注意が必要
交絡因子は網羅的に検討されているか?
概ねされている
Baseline は同等か?
概ね同等
ITT 解析されているか?
mITT解析(FAS)
追跡率(脱落)はどのくらいか?結果を覆す程か?
患者の 56.6%で中止され、45.0%は追跡できなかった。かなり脱落が多い。試験からの脱落(解析には含めない対象)としては全体で 8名。これはランダム割付後に治療を受けなかったため解析から除外された。
サンプルサイズは充分か?
イベント数 656と充分。 真のハザード比 =1.0、power =90で、624件のイベントが起きるよう設定された。中間解析はイベントが約 25、50、75%に達した時に行った。 2016年 4月には、75%暫定分析の時点で、推定されたハザード比と、信頼区間の調整された上限は、それぞれ 0.99と 1.23だった。しかし、ITT分析における任意の原因による死亡のハザード比と治療中に発生したイベント分析との間に不一致が認められたため、データおよび安全性監視委員会は、イベントが 624件発生するまで試験を遂行することを推奨した。
結果は?
6190名が解析対象となった。 フェブキソスタット群では、患者の 61.0%が 40mg、39.0%が 80mg/日の用量で服用した。 アロプリノール群では、推定クレアチニンクリアランスに基づいて、患者の 21.8%が 200mg、44.6%が 300mg、25.2%が 400mg、4.3%が 500mg、4.1%が 600mgの用量で服用した。 患者の 56.6%が早期に試験治療を中止した。 割合は、フェブキソスタット群とアロプリノール群でそれぞれ 57.3%と 55.9%と同等であった。 試験を完遂しなかった患者の割合は、フェブキソスタット群で 45.0%、アロプリノール群で 44.9%。全体で 45.0%であった。 フェブキソスタットの暴露期間の中央値は 728日。アロプリノール暴露の中央値は 719日であった。 フォローアップ期間の中央値は、フェブキソスタット群で 968日、アロプリノール群で 942日であった。
プライマリー・アウトカム
フェブキソスタット群 335イベント(10.8%) vs. アロプリノール群 321(10.4%) HR =1.03(97%CI 0.87-1.23)95.5-98.5% ARR = -0.4%、NNH =250 P =0.002 for 非劣性
セカンダリー・アウトカム
心血管死 F群 134(4.3%) vs. A群 100(3.2%) HR =1.34(95%CI 1.03-1.73) ARR= -1.1%、NNH=91 非致死性心筋梗塞 F群 111(3.6%) vs. A群 111(3.8%) HR =0.93(95%CI 0.72-1.21) ARR= 0.2%、 NNT =500 非致死性脳卒中 F群 71(2.3%) vs. A群 70(2.3%) HR =1.01(95%CI 0.73-1.41) ARR= 0.0% 不安定狭心症による緊急の血行再建術 F群 49(1.6%) vs. A群 56(1.8%) HR =0.86(95%CI 0.59-1.26) ARR= 0.2%、NNT =500 3-Point MACE F群 296(9.6%) vs. A群 271(8.8%) HR =0.86(95%CI 0.59-1.26) ARR= -0.8%、NNH =125 全死亡 F群 243(7.8%) vs. A群 199(6.4%) HR =1.22(95%CI 1.01-1.47) ARR= -1.4%、NNH =72
コメント
今回の試験はフェブリク®️(フェブキソスタット)の安全性検証をメインとしている。心血管イベントについてプライマリー・アウトカムは非劣性。つまりザイロリック®️(アロプリノール)とフェブキソスタットは、心血管イベントにおいて差が無い。しかし、セカンダリー・アウトカムである心血管死と全死亡では、フェブキソスタットの方が効果推定値は大きかった(つまり害が大きいかもしれないということ)。ちなみに資金提供は Takedaさん。 あくまで仮説生成ではあるが、ハードアウトカムに差が認められると個人的には敏感になってしまいます。アロプリノールで良くない?と言いたい私がいる。またアロプリノールは過去の臨床試験結果から、腎障害進行抑制や死亡率低下の可能性が示唆されている。こちらについては、また今度。
なんといっても脱落多いですよね。
-Evidence never tells you what to do-
👇 ポチッていただけますと喜びます。 ![]() にほんブログ村]]>
にほんブログ村]]>

コメント
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… […]
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… […]
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… […]
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… […]
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… Critical appraisal 批判的吟味 ランダム化比較試験 Randomized Controlled Trial Random 尿酸 Uric acid 高尿酸血症 hyperurecemia 痛風 Gout スポンサーリンク シェアする Twitter Facebook はてブ Pocket LINE コピー konyanko13をフォローする konyanko13 猫薬プロジェクト3rd〜論文情報の活用〜 […]
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… […]
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… […]
[…] 【批判的吟味】心血管疾患を伴う痛風患者に対してフェブリク®️とザ… […]